Už samotné bílkoviny, základní stavební kameny našeho těla, obsahují aromatické aminokyseliny. Jednou z nich je tyrosin, jehož postranní řetězec nese fenolový motiv, což je ideální model pro studium těchto interakcí. Na druhé straně stojí kationty, například neurotransmiter acetylcholin. Ten se podílí na řízení paměti, spánku i pohybu. Když se acetylcholin váže na své receptory, hraje v tom důležitou roli právě kation-π interakce. Dále nikotin, látka, která je považována za jednu z nejnávykovějších látek vůbec, se váže na nikotinové acetylcholinové receptory kation-π interakcí a muskarin, jed z muchomůrky červené, se váže stejným způsobem na muskarinové acetylcholinové receptory.
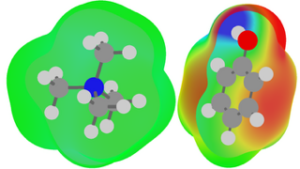
Přestože jsou kation-π interakce nesmírně důležité pro fungování biologických systémů, jejich chování ve vodném prostředí, kde se odehrává život, zatím není zcela pochopeno. V našem výzkumu jsme se proto zaměřili na co nejjednodušší model zachovávající biologickou relevanci, a to na interakci mezi tetramethylamonným kationtem, strukturně příbuzným acetylcholinu, a fenolem, který je součástí postranního řetězce aminokyseliny tyrosinu.
Pomocí kombinace experimentů a počítačových simulací jsme ukázali, že vazba mezi tetramethylamonným kationtem a fenolem je ve vodě stabilnější, než se dříve předpokládalo. Výsledky našeho výzkumu naznačují, že kation-π interakce mohou v biologických systémech hrát výraznější roli, než se dosud myslelo. Tyto poznatky tak přispívají k lepšímu pochopení základních molekulárních interakcí a mohou být inspirací i pro oblasti, jako je vývoj nových léčiv nebo inženýrství nových materiálů. Například v oblasti metal-organických sítí, za jejichž objev byla v roce 2025 udělena Nobelova cena za chemii.